(画像は生成AIを用いて作成しています。)
記事の概要:この記事ではGMP指摘事例速報 (オレンジレター) に記載されている内容をまとめ、AI活用によるリスク低減方法を解説します。
目次
GMP指摘事例速報 (オレンジレター)とは
医薬品は人の健康に直接影響するため、日本では製造する会社と販売する会社の役割を分け、厳しい許可制度で管理しています。製造販売としての許可を受けた会社は、医薬品を市場に出す最終責任者であり、品質の確認、安全性情報の収集、副作用の監視などを行います。実際の製造は工場に委託できますが、その責任は製造販売の会社に残ります。一方、工場側は「製造業許可」を受け、決められた基準 (GMP) に従って適切に製造しているかを査察されます。
これらの仕組みを専門的に支えているのが、PMDA (医薬品医療機器総合機構) です。PMDAは、医薬品が効果と安全性の両方を満たしているかを審査し、工場がルール通りに製造しているかを査察により確認します。また、市販後に起きた副作用の情報を集め、必要に応じて注意喚起を行います。つまりPMDAは、国と一緒に医薬品の品質と安全を守る「科学的な監視役」です。
GMP指摘事例速報 (オレンジレター)とは、PMDAが 2022 年から公表を始め、その目的は「業界全体への周知と改善促進」です。各オレンジレター本文は PDF で事例の背景・確認事例・問題点・チェックポイント・PMDA のメッセージが整理されています。
品質確保に関する取り組み | 独立行政法人 医薬品医療機器総合機構
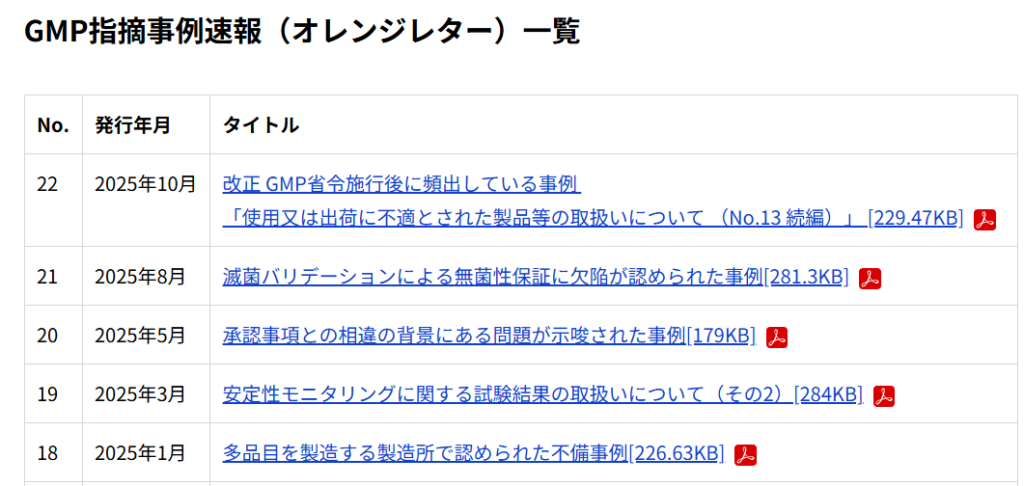
GMP指摘事例速報 (オレンジレター)の発行内容
各オレンジレターに記載されている内容を要約したのが以下の表です。
GMP省令と照らし合わせて、非常に幅広く指摘事例が紹介されていることがわかります。
| No. | 発行月 | 要約 | 指摘内容の要点 |
| 1 | 2022/4 | 原料の適正確認の重要性 | 原料ラベル確認がずさんで、受入記録が虚偽や作り物のような形跡があり、原料取り違えのリスクが高まっている。 |
| 2 | 2022/5 | 未知の薬理作用物品取り扱い | 薬理作用・毒性不明な物質を扱うのに、残留管理や毒性評価が不十分で安全性リスクを適切に評価できていない。 |
| 3 | 2022/7 | CAPA不足によるリスク見落とし | CAPA(是正・予防措置)が形だけで、出荷済みロットへの影響や再発防止策を十分に評価しておらず品質リスクを見落としている。 |
| 4 | 2022/9 | 委託管理(外部委託)不徹底 | 委託先管理が不徹底で、製造・試験を外部に任せつつ仕様や品質保証のチェックが甘く、委託リスクを低く見積もっている。 |
| 5 | 2022/12 | 不適切な記録作成 | 製造や試験記録の改ざん・不整合があり、真正な業務履歴を反映していない可能性があり、信頼性が損なわれている。 |
| 6 | 2022/12 | 指図に沿った記録にするための不適切修正 | 指示どおりの作業記録を装うために記録を後修正・バックデートし、不正確な手順の適用を隠蔽してしまっている。 |
| 7 | 2023/3 | 手順書不遵守によるリスク | 手順書通りに現場が動いておらず、標準作業手順(SOP)との乖離が常態化して、作業の不整合リスクがある。 |
| 8 | 2023/6 | 無菌操作区域の環境モニタリング不足 | 無菌操作区域での環境モニタリングが不十分、モニタリング頻度や手順不備で汚染リスクが高まっている。 |
| 9 | 2023/7 | 安定性モニタリングの試験結果の扱い | 安定性試験データのばらつきを軽視し、都合よい結果ばかりを採用。品質トレンドの異常に対する対応が不十分。 |
| 10 | 2023/10 | 組織内コミュニケーション(製造→経営) | 製造現場から経営層への報告が不十分で、品質問題の重要性が十分に伝わらず、迅速な対策が取れない。 |
| 11 | 2023/10 | 組織内コミュニケーション(経営→製造) | 経営層が製造管理状況を把握しておらず、GMPシステムが機能不全に陥っている可能性がある。 |
| 12 | 2024/1 | リスクに応じたバリデーション計画 | 品質リスクを適切に評価しないまま、バリデーション計画を作成。リスクに応じた検証が欠けている。 |
| 13 | 2024/3 | 不適品の取扱い(隔離等) | 不適品(出荷不可品)の保管・隔離があいまいで、良品と混在するリスクがある。管理手順も不十分。 |
| 14 | 2024/6 | 変更管理の要否判断 | 試験方法変更時に影響評価を省略。新しい分析条件でも品質が保たれているか検証されておらず、誤判定の恐れ。 |
| 15 | 2024/9 | 後発薬関連製造所の不備 | 後発薬工場でOOS(仕様逸脱)発生後の原因究明が不十分。品質第一より出荷優先の傾向が見られる。 |
| 16 | 2024/10 | 承認事項不遵守・虚偽記録 | 虚偽記録を作成し、上司・経営層も関与。承認条件や手順を遵守せず品質問題の報告もされていない。 |
| 17 | 2024/12 | リスクに応じた洗浄バリデーション | 洗浄バリデーションで共用設備のリスク評価がない。異品種混入や交差汚染の可能性を十分に考慮していない。 |
| 18 | 2025/1 | 多品目製造所での不備 | 多品目工場で作業手順・責任分担が混乱。切り替えミスや管理不備で品質リスクが拡大している。 |
| 19 | 2025/3 | 安定性モニタリング | 安定性モニタリングで異常傾向が見られても、報告・対応体制が未整備。都合の良い結果のみ重視されている。 |
| 20 | 2025/5 | 承認事項との相違が示唆される事例 | 承認内容(承認書)と実際の製造実態が異なる。試験を省略・変更し、承認条件未遵守の恐れ。 |
| 21 | 2025/8 | 滅菌バリデーションによる無菌性保証欠陥 | 滅菌バリデーションでBI種の妥当性が担保されておらず、無菌性保証レベルが不明確。検証データも管理不十分。 |
| 22 | 2025/10 | 改正GMP省令後に頻出する事例(不適品取扱い続編) | 不適品をロープ区切りの倉庫に放置、QA報告なしに廃棄。適切な隔離・報告手順が欠如して危険性がある。 |
生成AIでのリスク低減アプローチ
指摘事項について問題となった点の本質を考えた上で、生成AIを活用することでリスク低減するアイデアを以下に記載します。
安定性試験データのばらつきの軽視
安定性試験では、データのばらつきや異常傾向を適切に評価できないと、市場に出た後に品質劣化が発覚する重大リスクにつながります。製品の特性と統計的な解析手法を熟知しておく必要があり、高度な専門性が求められます。
この部分に生成AIを活用するには、過去の安定性試験データから製剤特性ごとの典型的な劣化パターンを学習させ、逸脱傾向を早期に検知するといったアプローチが考えられます。特に、取得データ数が少ない品目に対しても、類似製剤の挙動を参照して、比較基準を補完できる点が強みとなります。また、古典的な管理図の手法のみならず、機械学習により品質を予測するモデルを構築し、実測値と予測値の乖離が発生した際に調査を開始することで、従来の品質管理手法よりも高度に品質低下の要因分析が行われることが期待できます。
生成AIは、要注意ロットや劣化初期のサインをいち早く検出し、データのばらつきや傾向を人が分かりやすい形で可視化し、品質保証に一貫した判断基準を提供する役割が期待できます。
経営層が製造・品質状況を把握できない問題
経営層が現場の品質リスクをリアルタイムに把握できていない状態では、GMPシステム全体が形骸化しやすくなります。これまでは製造、QA、QCそれぞれに適切な管理者を設定し、組織として品質マネジメントシステムを運営していくことで医薬品の品質を守ってきました。
この領域に生成AIを当てはめることで、従来は膨大で扱いきれていなかったあらゆるデータを適切に管理できる状態になることが可能になります。現場から上がる膨大な製造記録や試験記録、逸脱報告、是正措置、変更管理、設備トラブルなどのデータを統合することが可能です。リスクの高い項目を経営層向けに要点を絞ってAIが伝えます。
特に自然言語での問いかけに対し「いま最も重要な品質リスクは何か」、「どの工場でCAPA停滞が起きているか」などを即座に判断するダッシュボードを構築することで、現場と経営層のコミュニケーションが円滑に進むことが期待できます。
洗浄バリデーションの不十分なリスク評価へのAI活用
交差汚染リスクの高い共用設備では、洗浄バリデーションにおけるリスク評価、清浄度評価が不十分だと、深刻な品質事故につながる恐れがあります。
生成AIは、製剤成分の物性や溶解性、設備の材質ごとの吸着性、過去の清浄度評価データなどを組み合わせることで、各品目の残留しやすさをモデル化することが期待できます。これにより、新たな品目を共用設備に追加する際に、過去の洗浄実績を参照しながら、洗浄条件やリスクの高い組み合わせを自動で提示できる可能性があります。
また過去の洗浄バリデーションの記録をAIに読み込ませ、傾向分析や課題のある工程を抽出することで、属人的判断に依存しないリスクベースアプローチが可能になります。AIを活用することで、洗浄バリデーションの設計を人に依存せず、データに基づく根拠のあるものへと進化させることが期待できます。
まとめ
PMDAから発行されているGMP指摘事例速報 (オレンジレター)をもとに、GMP領域に生成AIを活用することで、医薬品の品質をより高度に守るアプローチを考察してみました。
製薬企業における生成AI導入を力強くサポートするのが、私たち株式会社EQUESです。

・東京大学松尾研究室出身のAIの専門家のメンバーを中心に設立
・ISO/IEC 27001:2022認証取得:国際的な基準で安心のセキュリティ体制
私たちは単に技術を提供するだけでなく、お客様の隣で一緒に走り続ける「伴走型技術開発」を最も大切にしています。
課題発見から内製化まで一貫してサポート
弊社の強みは、戦略立案から開発、そして最終的な内製化まで、AIプロジェクトの全フェーズを一気通貫でご支援できる点にあります。
・AIDX寺子屋:

「社内に専門家がいない」というお悩みに応えるサービスです。月額10万円から、東大出身のAI専門家集団にチャットでいつでも相談し放題。ベンダー選定のセカンドオピニオンとしてもご活用いただけます。
・ココロミ (PoCサービス):
「まずは小さく試したい」というニーズに応え、月々250万円から本格的なPoC(概念実証)を実施。リスクを抑えながらAI導入の第一歩を踏み出せます。
・製薬SaaS QAI Generator:

特に弊社の強みである製薬分野では、品質保証(GMP)の文書作成業務を効率化するSaaSも提供。GENIACにも採択されるなど、高い評価をいただいています。
AI導入のパートナー選びで迷われているなら、ぜひ一度、私たちEQUESにご相談ください。お客様の課題に真摯に寄り添い、最適な解決策をご提案します。




